
导语:结直肠癌(CRC)是全球第三大常见癌症,也是癌症相关死亡的第二大原因,每年造成超过93.5万人死亡。微卫星稳定(MSS)或错配修复功能正常(pMMR)的结直肠癌是转移性结直肠癌(mCRC)病例中最常见的亚型,却因其免疫抑制性肿瘤微环境(TME)和低突变负担(TMB)而抵抗免疫检查点抑制剂(ICIs),犹如隐藏在一片“免疫沙漠”之中。2025年 6月,福建医科大学研究团队在期刊《Advanced Science》上发表了研究论文,带来了一种全新的组合疗法,成功绿化了这片“沙漠”。
一、 微卫星稳定型结直肠癌面临的困境
“微卫星”指真核生物基因组中由1-6个核苷酸串联重复构成的DNA序列,其不稳定性(MSI)与多种癌症相关。在结直肠癌中,微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)肿瘤占转移性病例的5%–10%,具有高肿瘤突变负荷(TMB),容易被免疫系统发现和攻击;相比之下,微卫星稳定型(MSS)或错配修复功能正常(pMMR)的结直肠癌占转移性病例的90%–95%,却因在基因组微卫星位点上未表现出不稳定性、且错配修复蛋白表达正常(pMMR),形成了以低TMB等为特征的免疫抑制性肿瘤微环境(TME),产生的新抗原不足,无法引起 T 细胞的识别,导致对ICIs几乎完全不敏感,使之成为一片免疫治疗的“沙漠”。
因此,本研究旨在用“个性化新抗原疫苗(Neo-CRCVAS)”+“靶向药瑞戈非尼(Regorafenib)”,作为一种新疗法(RegoNeo),重塑微卫星稳定结直肠癌肝转移(MSS-CRLM)的肿瘤微环境(TME)并增强肿瘤免疫原性,克服免疫抵抗,将“沙漠”恢复成“绿洲”(图1)。
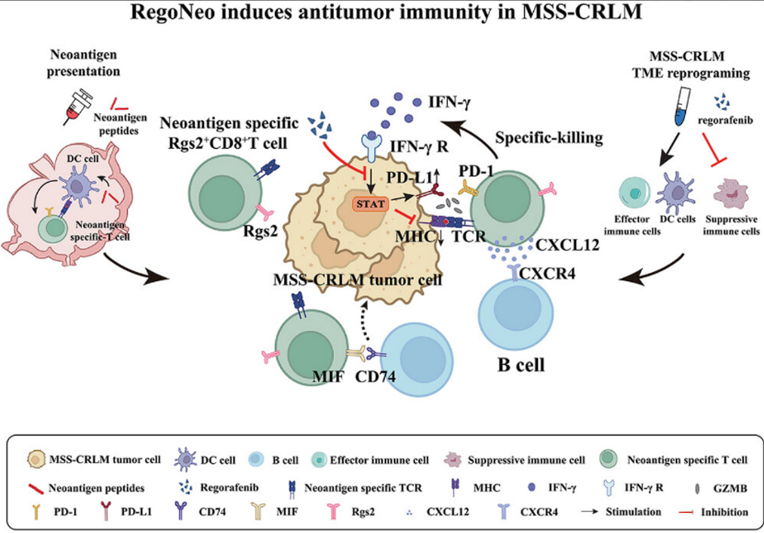
图1 RegoNeo诱导MSS-CRLM抗肿瘤免疫机制
二、 开发疫苗:新抗原的筛选与验证
研究人员首先对小鼠 MSS-CRC cmt93 细胞和 C57BL/6 正常组织进行了全外显子测序和转录组测序,随后进行生物信息学算法分析和动物免疫原性验证,最终筛选出了引发免疫反应最显著的 7 个新抗原肽,并与 Poly (I:C) 佐剂合成个性化新抗原疫苗 (Neo-CRCVAS),能诱导小鼠产生特异性免疫响应,且与野生肽段无交叉反应,安全性好,为后续应用奠定了基础(图2)。
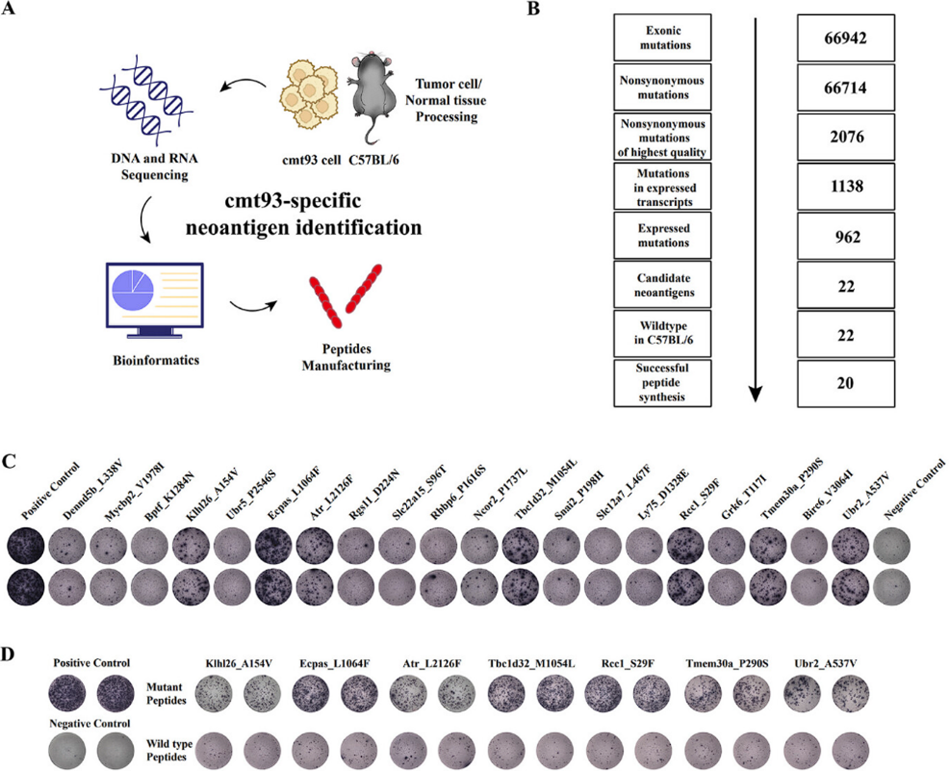
图2 新抗原鉴定与免疫原性验证
三、 测试疗效:Neo-CRCVAS在小鼠模型中展现出特异性抗肿瘤作用
为评估Neo-CRCVAS的抗肿瘤疗效,研究人员建立了MSS-CRLM小鼠模型并接种疫苗。结果显示,单用Neo-CRCVAS治疗的确能使肿瘤消退,但未能完全抑制肿瘤生长:60%的Neo-CRCVAS治疗小鼠表现出抗药性或在初步缓解后继续进展。因此,研究人员进一步分析了小鼠肿瘤微环境的免疫变化,发现免疫抑制性的微环境通过限制淋巴细胞浸润、耗竭效应型免疫细胞、下调抗原提呈能力等途径诱导免疫逃逸(图3)。
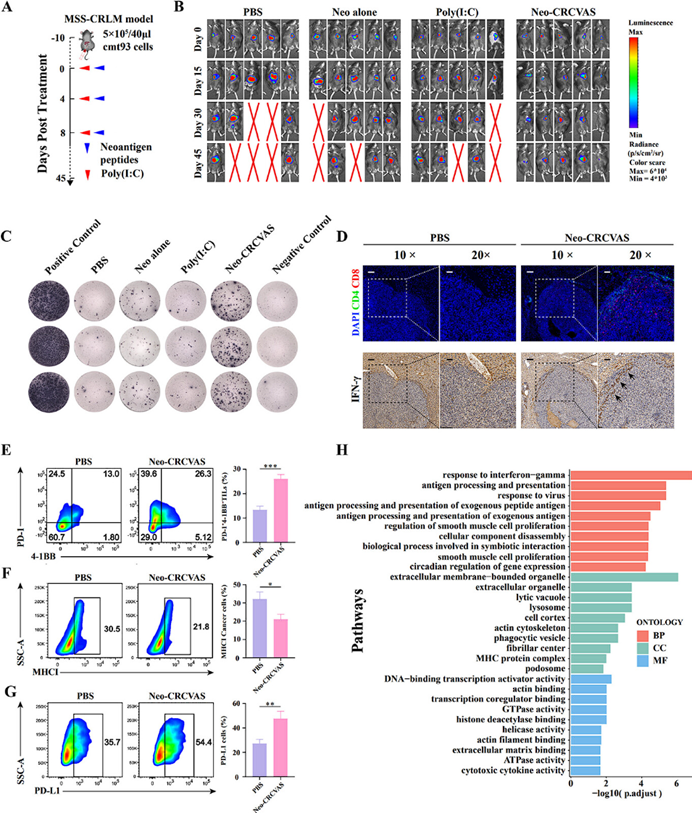
图3 MSS-CRLM小鼠模型中Neo-CRCVAS的抗肿瘤疗效及潜在耐药机制
四、 优化提升:Neo-CRCVAS联合瑞戈非尼增强抗肿瘤免疫反应
瑞戈非尼(Regorafenib)是唯一已知能增强免疫细胞浸润并逆转 IFN-γ 诱导的MHC 下调和PD-L1上调的多靶点酪氨酸激酶抑制剂,能增强抗肿瘤免疫反应。研究团队发现,Neo-CRCVAS与瑞戈非尼的联合疗法(RegoNeo)促进了新抗原特异性T细胞浸润肿瘤,可有效刺激强烈的免疫反应,实现了小鼠模型80%的持续肿瘤退化率和100%的生存率(图4)。
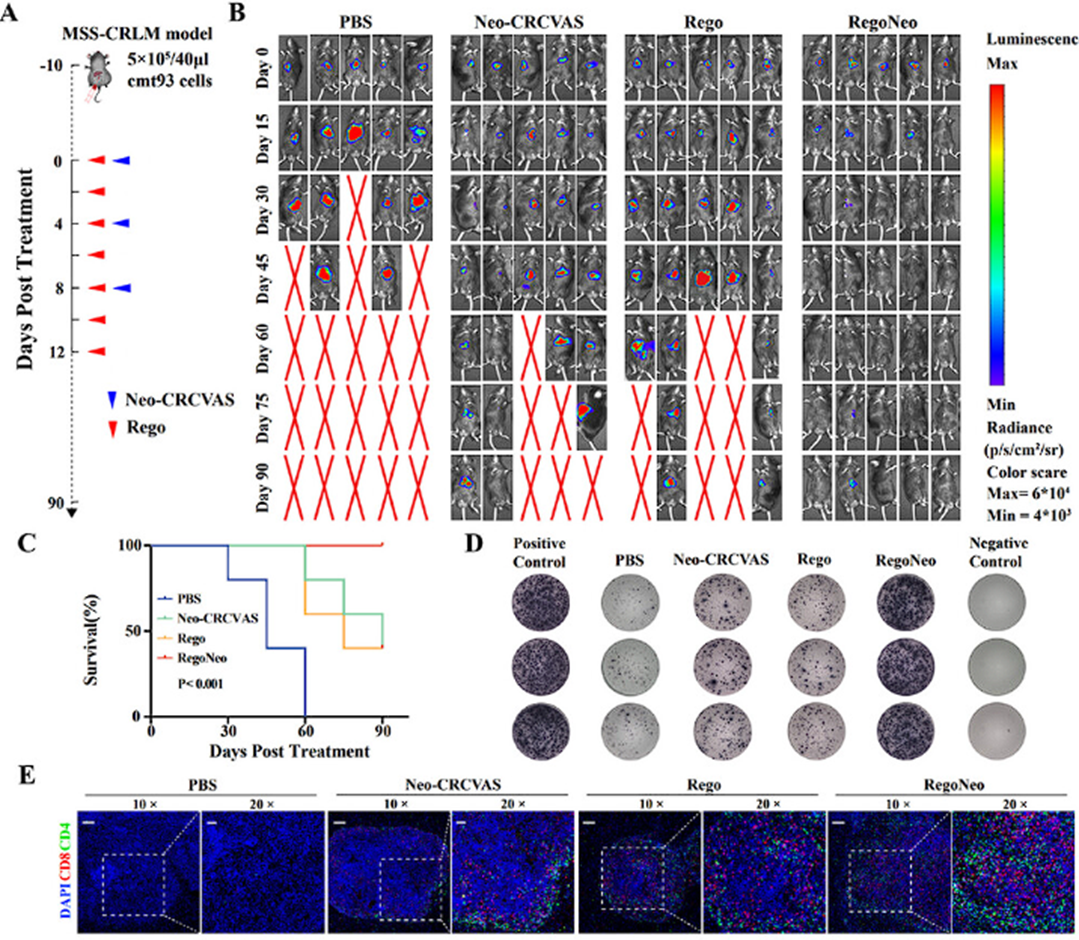
图4 RegoNeo在MSS-CRLM小鼠模型中的抗肿瘤疗效
此外,研究人员还发现 RegoNeo 不仅能促进肿瘤消退,还能激发持久的免疫记忆。在向 RegoNeo 治愈的小鼠重新注射肿瘤细胞以模拟CRLM的转移时,6只小鼠中有5只肿瘤未出现生长,而所有对照组小鼠肿瘤负荷均迅速增加;酶联免疫斑点法检测(ELISPOT)显示,小鼠脾T细胞在治疗后第50天对新抗原肽仍保持显著敏感性。这说明 RegoNeo 诱导了长效免疫记忆,能够有效预防复发转移(图5)。
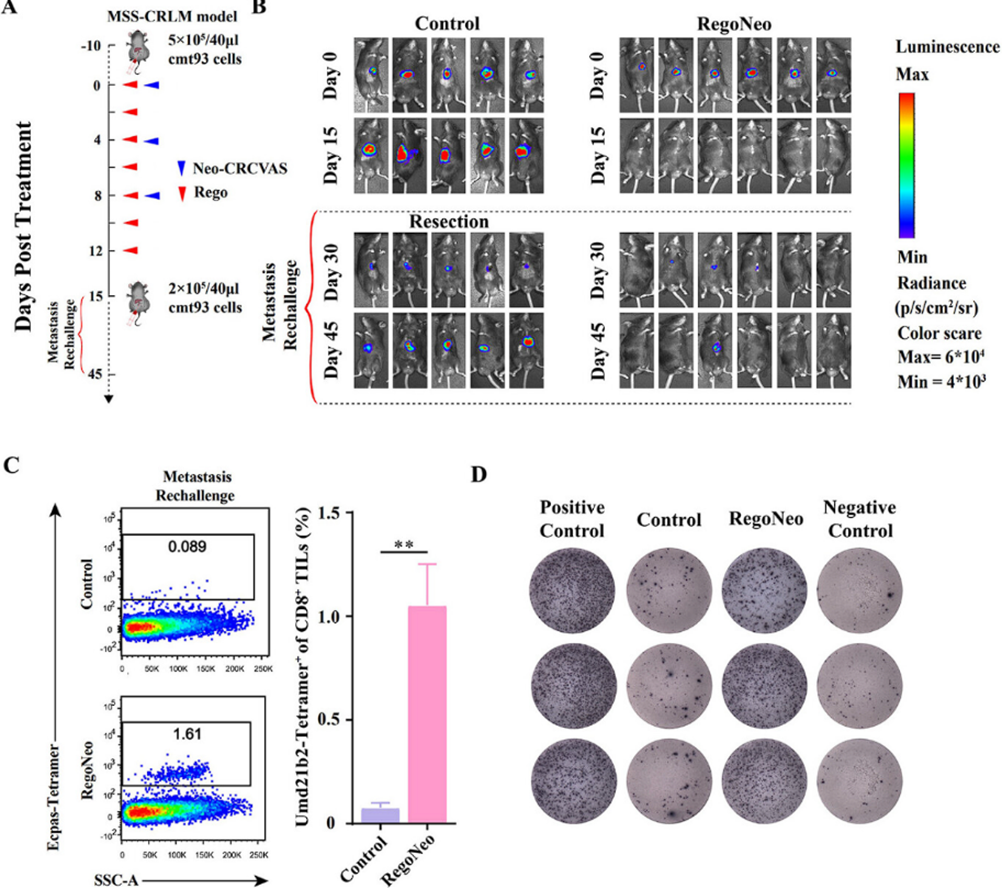
图5 体内 RegoNeo 治疗的转移再挑战
五、 机制探究:RegoNeo 的协同效应从何而来?
为了探索 RegoNeo 发挥强效抗肿瘤效果的潜在机制,研究人员对 RegoNeo 治疗后MSS-CRLM 模型 TME 的免疫状态变化进行了分析。单细胞测序数据显示,RegoNeo处理组的调节性 T 细胞(Tregs)和耗竭性 T 细胞(Tex)明显减少,而 Rgs2+CD8+ T细胞显著富集,并表现出相对较高的肿瘤坏死因子(TNF,一种关键的促炎细胞因子)表达,提示免疫系统的激活;同时,RegoNeo处理组也显示出最多的T细胞抗原受体(TCR)克隆型,说明治疗诱导了TCR型变异和扩增,这可能新抗原的特异性免疫相关(图6)。
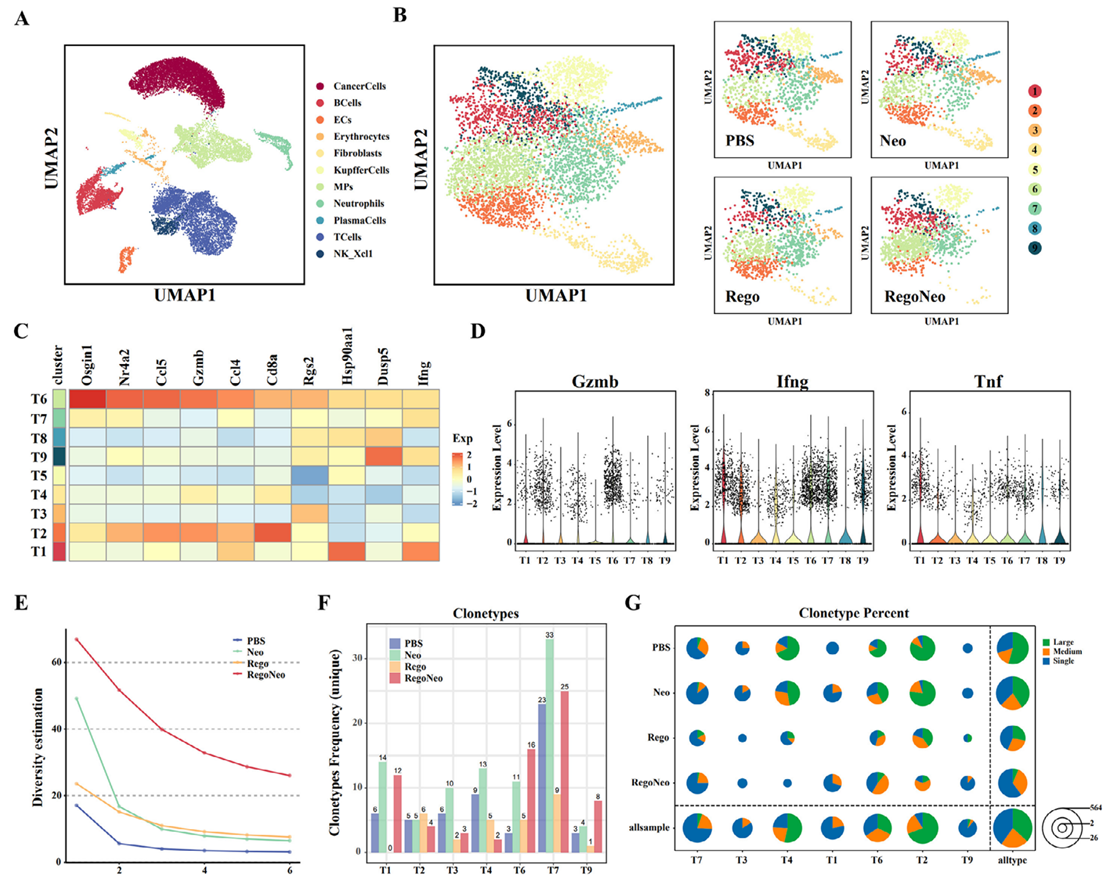
图6 通过scRNA-seq数据对RegoNeo处理后免疫微环境的表征
六、 疗效验证:多维度证实MSS-CRLM治疗中Rgs2+CD8+ T细胞抗肿瘤潜力
最后,研究人员从 RegoNeo 治疗的MSS-CRLM小鼠模型或新鲜切除的CRLM患者肿瘤组织中分离出Rgs2+CD8+ T细胞和Rgs2-CD8+ T细胞,并从多个维度评估其肿瘤杀灭能力:
l 体外:与 cmt93 肿瘤细胞共培养,Rgs2+CD8+ T细胞共培养组的凋亡细胞水平升高。
l 体内:静脉注射到 MSS-CRLM 小鼠中,接种Rgs2+CD8+ T细胞的小鼠肿瘤负荷显著低于对照组和Rgs2−CD8+ T细胞组。
l 临床样本:与 MSS-CRLM 患者肿瘤组织衍生的类器官(PDOs)共培养,Rgs2+CD8+ T细胞共培养组中PDOs的凋亡率增加(图7)。
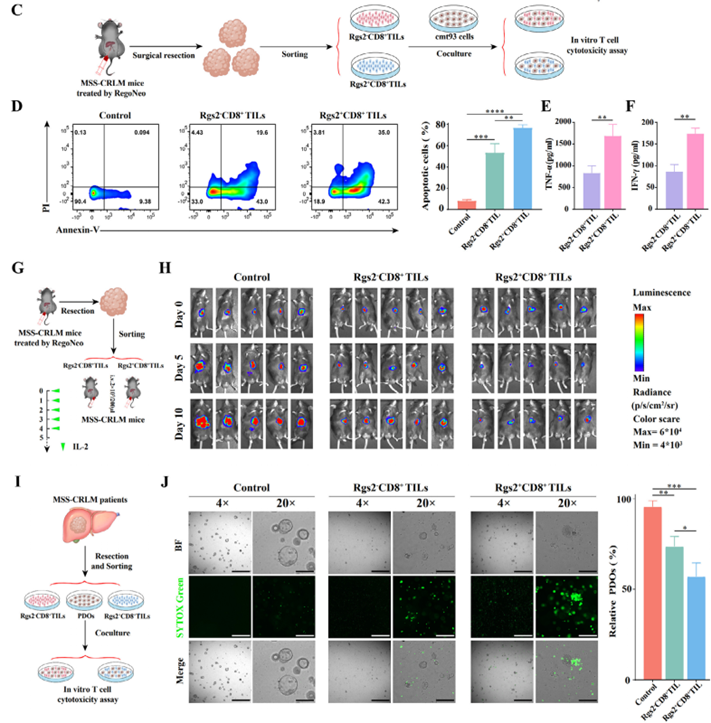
图7 Rgs2+CD8+ T细胞的浸润及抗肿瘤疗效
七、 总结
l 本研究开发了个性化新生抗原疫苗 Neo-CRCVAS 与瑞戈非尼的联合治疗策略(RegoNeo),通过诱导具有新抗原特异性的Rgs2+CD8+ T细胞浸润,从而激活抗肿瘤反应,并建立了持久的肿瘤特异性免疫记忆,为微卫星稳定型结直肠癌肝转移的精准治疗提供了新的思路。
l “新抗原疫苗找目标,靶向药开道,免疫细胞攻坚”——在更多类似的低突变负荷、低免疫浸润或伴有特定驱动基因突变的“冷肿瘤“中,此类个性化策略将提供更加精准的治疗方案,惠及更多免疫耐受的肿瘤患者。
该研究采用传统基因测序和预测方法寻找肿瘤新抗原,Rapid Novor 快序生物提供蛋白从头测序服务,可直接、精准、高效地鉴定所有突变来源的新抗原肽段,不仅能对传统方法查漏补缺、提供证据支持,还能发现更多隐匿的突变靶点,让治疗方案变得更强大、覆盖更多人。
参考文献
Chen H, Chen B, Yang Y, et al. Personalized Neoantigen Vaccine plus Regorafenib Increases Rgs2⁺CD8⁺ T Cells Infiltration and Reprograms the Tumor Microenvironment in Microsatellite Stable Colorectal Cancer Liver Metastases. Adv Sci (Weinh). 2025 Sep;12(36):e08040. doi: 10.1002/advs.202508040.